Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
бензо[c]фурандион
Синонимы и иностранные названия:
phthalic anhydride (тривиальное, англ.)
орто-фталевой кислоты ангидрид (рус.)
фталевой кислоты ангидрид (тривиальное, рус.)
фталевый ангидрид (рус.)
Тип вещества:
органическое
Внешний вид:
бесцветн. игольчатые кристаллыБрутто-формула (по системе Хилла для органических веществ):
C8H4O3Формула в виде текста:
C6H4(CO)2OМолекулярная масса (в а.е.м.): 148,12
CAS №: 85-44-9
Температура плавления (в °C):
130,95 [Лит.]
Температура возгонки (сублимации) (в °C):
284,5
Растворимость (в г/100 г растворителя или характеристика):
1,1,2-трифтор-1,2,2-трихлорэтан: растворим [Лит.]
ацетон: растворим [Лит.]
бензол: растворим (80°C) [Лит.]
вода: 0,00295 (0°C) [Лит.]
вода: 0,62 (26,7°C) [Лит.]
вода: 1,63 (50°C) [Лит.]
вода: реагирует (100°C) [Лит.]
диэтиловый эфир: мало растворим [Лит.]
муравьиная кислота 95%: 4,67 (19,8°C) [Лит.]
пиридин: 83,5 (20°C) [Лит.]
сероуглерод: 0,013 (-112,5°C) [Лит.]
сероуглерод: 0,03 (-40°C) [Лит.]
сероуглерод: 0,2 (0°C) [Лит.]
сероуглерод: 0,3 (10°C) [Лит.]
сероуглерод: 0,7 (20°C) [Лит.]
сероуглерод: 1,7 (60°C) [Лит.]
этанол: растворим [Лит.]
Плотность:
1,527 (20°C, г/см3, состояние вещества - кристаллы)
Нормативные документы, связанные с веществом:
- ГОСТ № 32457-2013 "Фталевый ангидрид. Определение содержания в воздушной среде методом газовой хроматографии - масс-спектрометрии"
- ГОСТ № 32532-2013 "Фталевый ангидрид. Определение содержания в воздушной среде полярографическим методом"
- Приказ государственного комитета Российской Федерации по рыболовству № 96 от 28.04.1999 "О рыбохозяйственных нормативах" (Описание документа: ПДК и ОБУВ для водных объектов, имеющих рыбохозяйственное значение.)
- предельно допустимая концентрация (мг/л) в природной воде = 0,05 (токсикологический показатель)
Способы получения:
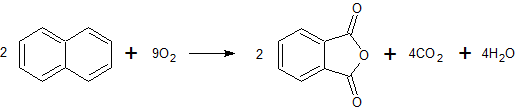
- Окисление нафталина сульфатом ртути(II) в серной кислоте. [Лит.]
- Промышленно фталевый ангидирид получают окислением нафталина кислородом воздуха при нагревании до 435-450 С над катализатором (оксид ванадия(V)). Название реакции: реакция Гиббса-Воля. [Лит.1
 , Лит.2]
, Лит.2]
Используется для синтеза веществ:
3-нитробензол-1,2-дикарбоновая кислота
фталевой кислоты моноамид
Реакции вещества:
- Реагирует с фенилуксусной кислотой и ацетатом натрия с образованием бензальфталида. (выход 71%) [Лит.]
- Реагирует с бутанолом в присутствии серной кислоты с образованием дибутилфталата. [Лит.]
- При нагревании с глицерином дает смесь глифталевых смол. [Лит.]
- Конденсируется с резорцином давая краситель флуоресцеин. [Лит.]
- Реагирует с водным раствором аммиака с образованием аммониевой соли моноамида фталевой кислоты. [Лит.]
- При пропускании паров фталевого ангидрида и воды через сильно нагретый катализатор получают бензойную кислоту. [Лит.]
- Действием сухого аммиака на расплавленный фталевый ангидрид получают фталимид. [Лит.]
- В парах реагирует с аммиаком над катализатором с образованием 1,2-дицианобензола. [Лит.]
- С пентахлоридом фосфора образует дихлорангидрид фталевой кислоты. [Лит.]
- С диметилкадмием образует 3,3-диметилфталид. (выход 60%) [Лит.]
- В присутствии хлорида алюминия реагирует с бензолом с образованием о-бензоилбензойной кислоты. (выход 93,6%) [Лит.]
- Реагирует с трихлорацетатом натрия с образованием 3-гидрокси-3-трихлорметилфталида. (выход 80%) [Лит.]
- При кипячении с триэтилфосфитом дает дифталил. (выход 70%) [Лит.]
- Нагревание с тщательно очищенной цинковой пылью дает дифталил. [Лит.]
- С цинковой пылью в уксусной кислоте дает сложную смесь продуктов восстановления. [Лит.]
- Реагирует с малоновой кислотой в присутствии пиридина с образованием 2-ацетилбензойной кислоты. [Лит.]
- Реагирует с пропионовым ангидридом в присутствии пропионата калия с образованием 3-этилиденфталида. [Лит.]
- Реагирует с диэтилмалонатом с образованием диэтилового эфира фталидилиденмалоновой кислоты. [Лит.]
- Реагирует с цинком и иодметаном в течение 7-8 дней с образованием 3,3-диметилфталида. [Лит.]
- С реактивами Гриньяра образует о-ацилбензойные кислоты. [Лит.]
- Реагирует с уксусным ангидридом в присутствии ацетата натрия с образованием фталидилиденуксусной кислоты. [Лит.]
- Реагирует с толуолом в присутствии хлорида алюминия с образованием 2-(4-метилбензоил)бензойной кислоты. (выход 96%) [Лит.]
- При нагревании при 240 С с N-трет-бутилмочевиной дает N-трет-бутилфталимид, углекислый газ и аммиак. (выход 72%) [Лит.]
- Реагирует с фенилаланином в присутствии триэтиламина, при кипячении в толуоле, с образованием N-фталилфенилаланина. (выход 78%) [Лит.]
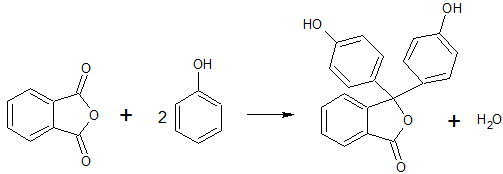
- Фенолфталеин получают конденсацией фенола и фталевого ангидрида в присутствии катализатора. Катализаторами являются хлорид цинка, его смесь с п-толуолсульфохлоридом, серная кислота, хлорид алюминия. Выход 93% (для хлорида цинка, с серной кислотой выход 25%, с хлоридом алюминия - 35%). [Лит.1
 (с H2SO4), Лит.2
(с H2SO4), Лит.2 (со смесью ZnCl2), Лит.3
(со смесью ZnCl2), Лит.3 (с H2SO4), Лит.4
(с H2SO4), Лит.4 (с AlCl3), Лит.5
(с AlCl3), Лит.5 (с H2SO4), Лит.6
(с H2SO4), Лит.6 (с H2SO4), Лит.7
(с H2SO4), Лит.7 (с H2SO4), Лит.8
(с H2SO4), Лит.8 (с H2SO4), Лит.9
(с H2SO4), Лит.9 (с ZnCl2), Лит.10
(с ZnCl2), Лит.10 (с H2SO4)]
(с H2SO4)]
- Фталевый ангидрид реагирует с иодом и 60% олеумом при нагревании до 65 С и дальнейшем нагревании при 170 С с образованием тетраиодфталевого ангидрида. Выход 80-82%. [Лит.1]
- 3-Нитрофталевую кислоту получают нитрованием фталевого ангидрида смесью азотной и серной кислот при нагревании. Выход 28-31%. [Лит.1
 , Лит.2
, Лит.2 ]
]
Дополнительная информация::
Легко возгоняется.
Источники информации:
- CRC Handbook of Chemistry and Physics. - 95ed. - CRC Press, 2014. - С. 3-460
- Seidell A. Solubilities of organic compounds. - 3ed., vol.2. - New York: D. Van Nostrand Company, 1941. - С. 569-570
- Yalkowsky S.H., Yan H. Handbook of aqueous solubility data. - CRC Press, 2003. - С. 445
- Гуревич Д.А. Фталевый ангидрид. - М.: Химия, 1968
- Мономеры для поликонденсации. - М.: Мир, 1976. - С. 412-413
- Ошкая В.П. Ангидридная конденсация. - Рига: Зинатне, 1973
- Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1977. - С. 190
- Справочник по растворимости. - Т.1, Кн.1. - М.-Л.: ИАН СССР, 1961. - С. 490-491
- Справочник по растворимости. - Т.1, Кн.2. - М.-Л.: ИАН СССР, 1962. - С. 1048
- Справочник химика. - 2 изд., Т. 2. - Л.-М.: Химия, 1964. - С. 1064-1065
- Физер Л., Физер М. Реагенты для органического синтеза. - Т. 4 (У-Я). - М., 1968. - С. 115-116
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер
![бензо[c]фурандион](DBimage/formula-gif/phtalic-anhydrid.gif)
![бензо[c]фурандион](DBimage/formula-gif/phtalic-anhydrid.gif)

