Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
фенолфталеин
Синонимы и иностранные названия:
α,α-ди(4-оксифенил)фталид (рус.)
phenolphthalein (англ.)
пурген (рус.)
Тип вещества:
органическое
Внешний вид:
бесцветн. ромбические кристаллы (растворитель перекристаллизации - этанол)Кристаллические модификации, структура молекулы, цвет растворов и паров:
Растворы бесцветны в кислой и сильнощелочной среде. В щелочной среде раствор имеет пурпурную окраску.
Брутто-формула (по системе Хилла для органических веществ):
C20H14O4Молекулярная масса (в а.е.м.): 318,32276
CAS №: 77-09-8
Температура плавления (в °C):
261Растворимость (в г/100 г растворителя или характеристика):
ацетон: 26,4 (18°C) [Лит.]
ацетон: 28,01 (25°C) [Лит.]
бензол: 0,16 (18°C) [Лит.]
бензол: 0,0031 (25°C) [Лит.]
вода: 0,0002 (25°C) [Лит.]
глицерин 95,2%: 0,053 (25°C) [Лит.]
диэтиловый эфир: 8,34 (20°C) [Лит.]
диэтиловый эфир: 0,48 (25°C) [Лит.]
керосин: 0,0019 (25°C) [Лит.]
ксилол: 0,18 (18°C) [Лит.]
метанол: 14,2 (18°C) [Лит.]
метанол: 9,17 (25°C) [Лит.]
метиламин: легко растворим [Лит.]
нитробензол: 4,41 (18°C) [Лит.]
петролейный эфир: 0,017 (25°C) [Лит.]
пиридин: 769 (при комнатной температуре) [Лит.]
пиридин: 152,29 (25°C) [Лит.]
сероуглерод: 0,18 (18°C) [Лит.]
тетрахлорметан: 0,0013 (25°C) [Лит.]
толуол: 0,61 (18°C) [Лит.]
уксусная кислота: 0,44 (25°C) [Лит.]
хлороформ: 3,06 (18°C) [Лит.]
хлороформ: 0,006 (25°C) [Лит.]
этанол: 26,5 (20°C) [Лит.]
этанол 41,5%: 0,78 (25°C) [Лит.]
этанол 92,4%: 10,37 (25°C) [Лит.]
этанол 99,6%: 9,2 (25°C) [Лит.]
этилацетат: 6,56 (18°C) [Лит.]
этиленгликоль: 2,14 (25°C) [Лит.]
Цвет растворов:
оранжев. (растворитель: серная кислота)
Плотность:
1,277 (32°C, г/см3, состояние вещества - кристаллы)
Вкус, запах, гигроскопичность:
запах: без запаха
Некоторые числовые свойства вещества:
Год открытия: 1871 (Байер)
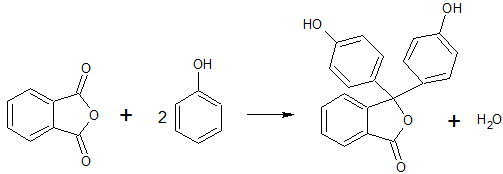
Метод получения 1:
Источник информации: Гитис С.С., Глаз А.И., Иванов А.В. Практикум по органической химии: Органический синтез. - М.: Высшая школа, 1991 стр. 255-256Смесь 5 г фталевого ангидрида, 10 г фенола и 2 мл концентрированной серной кислоты помещают в колбу и нагревают на масляной бане в течение 1,5 ч, строго соблюдая температуру 125...130°С (термометр в плаве) и периодически перемешивая содержимое. Горячую смесь выливают в колбу со 100 мл кипящей воды и отгоняют с водяным паром не вступивший в реакцию фенол. Во избежание разбрызгивания и связанной с этим потерей вещества жидкость нужно все время перемешивать. Раствору дают охладиться, после чего декантируют на воронку Бюхнера, стараясь по возможности не переносить осадок на фильтр. Затем продукт промывают декантацией двумя небольшими порциями холодной воды, присоединяют то, что все-таки попало на фильтр, к основной массе твердого вещества в стакан, растворяют в небольшом количестве теплого 4...5%-ного раствора гидроксида натрия и отделяют фильтрованием непрореагировавший фталевый ангидрид.
К темно-красному фильтрату прибавляют уксусную кислоту до полного осаждения фенолфталеина, после чего добавляют несколько капель соляной кислоты. Спустя 1 ч продукт отфильтровывают, сушат и перекристаллизовывают из водного спирта с использованием активированного угля.
Выход около 4 г (35 ...40% от теоретического).
Фенолфталеин [2,2-бис(п-гидроксифенил)фталид] — бесцветные ромбические иглы (перекристаллизация из разбавленного этилового спирта) с т. пл. 261 °С; трудно растворим в воде (0,018 г в 100 мл), хорошо— в этиловом спирте (20,9 г в 100 мл), умеренно — в диэтиловом эфире (5,92 г в 100 мл).
Метод получения 2:
Источник информации: Ошкая В.П. Ангидридная конденсация. - Рига: Зинатне, 1973 стр. 13Смесь 10 г (0,068 мол) фталевого ангидрида, 25 г (0,266 мол) фенола и 15 г (0,11 мол) безводного хлористого алюминия осторожно нагревают на масляной бане. Когда температура реакционной смеси достигает ~46°, начинается бурная реакция с выделением хлористого водорода. В течение 1 часа при медленном повышении температуры до 100° реакция завершается и реакционная смесь затвердевает. Остаток после перегонки полученного продукта с водяным паром экстрагируют сначала с разбавленной соляной кислотой для удаления хлористого алюминия, потом с разбавленным раствором едкого натра. Подкислением щелочной вытяжки разбавленной кислотой выделяют осадок фенолфталеина. Кристаллизуют из 70%-ного метанола.
Выход 35%.
Способы получения:
- Фенолфталеин получают конденсацией фенола и фталевого ангидрида в присутствии катализатора. Катализаторами являются хлорид цинка, его смесь с п-толуолсульфохлоридом, серная кислота, хлорид алюминия. Выход 93% (для хлорида цинка, с серной кислотой выход 25%, с хлоридом алюминия - 35%). [Лит.1
 (с H2SO4), Лит.2
(с H2SO4), Лит.2 (со смесью ZnCl2), Лит.3
(со смесью ZnCl2), Лит.3 (с H2SO4), Лит.4
(с H2SO4), Лит.4 (с AlCl3), Лит.5
(с AlCl3), Лит.5 (с H2SO4), Лит.6
(с H2SO4), Лит.6 (с H2SO4), Лит.7
(с H2SO4), Лит.7 (с H2SO4), Лит.8
(с H2SO4), Лит.8 (с H2SO4), Лит.9
(с H2SO4), Лит.9 (с ZnCl2), Лит.10
(с ZnCl2), Лит.10 (с H2SO4)]
(с H2SO4)]
Реакции вещества:
- При сплавлении с едким натром дает 4,4'-дигидроксибензофенон. [Лит.]
- При нагревании с концентрированной серной кислотой дает фенол и 2-гидроксиантрахинон. [Лит.]
- При действии щелочей раскрывает лактонное кольцо с образованием 2-[(4-оксоциклогекса-2,5-диен-1-илен)(4-натриооксифенил)метил]бензоата натрия пурпурного цвета, который в концентрированных щелочах обесцвечивается из-за образования неокрашенного 2-[гидрокси-бис(4-натриооксифенил)метил]бензоата натрия. [Лит.]
Показатели диссоциации:
pKa (1) = 9,4 (25°C, вода)
Анализ вещества:
 При добавлении щелочи водный раствор приобретает розовую окраску (см фото).
При добавлении щелочи водный раствор приобретает розовую окраску (см фото).
Применение вещества:
- кислотно-основной индикатор (интервал перехода окраски рН 8,2 (бесцветная) - 10,0 (красная)) [Лит.]
- лекарственное средство: слабительное [Лит.]
Неверная или противоречивая информация:
- Растворимость фенолфталеина в воде, равная 0,0175 г/100 г (Справочник химика т.2, Гитис), это ошибочная информация из-за путаницы с фенолфталином. [Лит.]
Источники информации:
- CRC Handbook of Chemistry and Physics. - 95ed. - CRC Press, 2014. - С. 3-446
- Dictionary of organic compounds. - Vol. 3, naphthacarbazole - zygadenine. - М.: ИИЛ, 1949. - С. 372
- The Merck Index 11th ed., Merck & Company, 1989. - С. 1150-1151
- Беликов В.Г. Учебное пособие по фармацевтической химии. - М.: Медицина, 1979. - С. 160
- Девяткин В.В., Ляхова Ю.М. Химия для любознательных, или о чем не узнаешь на уроке. - Ярославль: Академия Холдинг, 2000. - С. 53
- Индикаторы. - Т. 1. - Редактор Бишоп Э. - М.: Мир, 1976. - С. 135-136
- Справочник по растворимости. - Т.1, Кн.2. - М.-Л.: ИАН СССР, 1962. - С. 1249, 1371, 1526, 1585
- Справочник химика. - 2 изд., Т. 2. - Л.-М.: Химия, 1964. - С. 1052-1053
- Химическая энциклопедия. - Т. 5. - М.: Советская энциклопедия, 1999. - С. 74
- Энциклопедия для детей. - Т.17: Химия. - М.: Аванта+, 2004. - С. 163
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер


 При добавлении щелочи водный раствор приобретает розовую окраску (см фото).
При добавлении щелочи водный раствор приобретает розовую окраску (см фото).