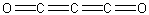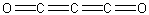Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
1,3-диоксопропадиен
Синонимы и иностранные названия:
carbon suboxide (англ.)
трикарбодиоксид (рус.)
триуглерода диоксид (рус.)
углерода недоокись (тривиальное, рус.)
Вещество входит в группы:
вещества необычного строения или состава
оксиды углерода
Тип вещества:
органическое
Внешний вид:
бесцветн. газБрутто-формула (по системе Хилла для органических веществ):
C3O2Формула в виде текста:
O=C=C=C=OМолекулярная масса (в а.е.м.): 68,03
Температура плавления (в °C):
-111,3Температура кипения (в °C):
7Растворимость (в г/100 г растворителя или характеристика):
вода: реагирует [Лит.]
диоксан: растворим [Лит.]
диэтиловый эфир: растворим [Лит.]
ксилол: растворим [Лит.]
сероуглерод: растворим [Лит.]
тетрагидрофуран: растворим [Лит.]
Плотность:
1,114 (0°C, г/см3, состояние вещества - жидкость)
Энергии, длины и углы связей молекул вещества:
Длина связи (пм): 116 (C=O)
Длина связи (пм): 128 (С=С)
Некоторые числовые свойства вещества:
Год открытия: 1906 (Дильс)
Метод получения 1:
Источник информации: Руководство по неорганическому синтезу. - Т.3, под ред. Брауэра Г. - М.: Мир, 1985 стр. 682-683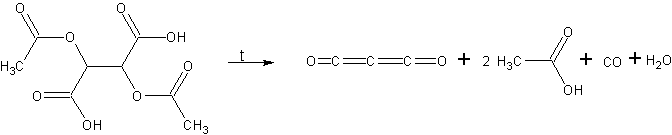
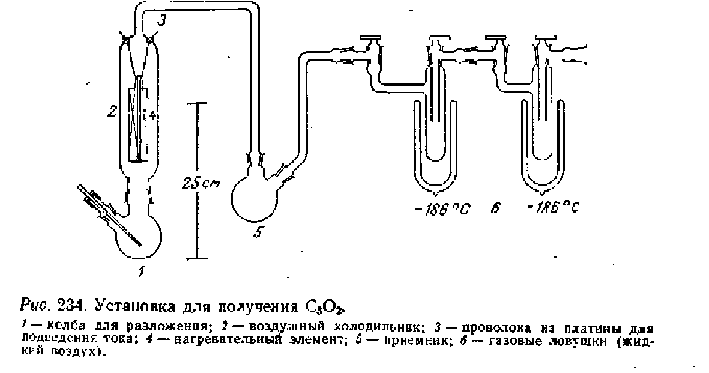
В колбу на 500 мл помещают 250 г ангидрида диацетилвинной кислоты (который должен быть предварительно промыт бензолом и высушен; т.пл. 120-130°С). На колбу через шлиф насаживают воздушный холодильник, в который впаяны две платиновые проволочки для подвода электрического тока. Ток подводится к нагревательному элементу, изготовленному из 2 м платиновой проволоки (диаметр 0,3 мм). К холодильнику присоединен первый охлаждаемый льдом сосуд. Продукты реакции конденсируются в охлаждаемых жидким воздухом ловушках с очень широкими трубками для подвода газа. Для того чтобы не было внезапного вскипания в колбе, в нее вводят капилляр. Установку эвакуируют, колбу нагревают на песчаной бане или плитке с закрытой спиралью до 200 °С и подают на нагревательный элемент электрический ток силой 4-4,5 А, доводя платиновый нагревательный элемент до температуры красного каления. Образующийся в результате реакции и неконденсирующийся угарный газ должен все время откачиваться, т. е. насос должен работать с такой нагрузкой, чтобы давление в установке всегда оставалось ниже 11 мм.рт.ст. Одновременно образующаяся уксусная кислота большей частью конденсируется в приемнике. Недокись углерода, содержащиая небольшое количество углекислого газа, вымораживают в последующих газовых ловушках. Выделяющийся из насоса угарный газ уничтожают путем сгорания в пламени бунзеновской горелки. За 6-8 ч разлагается около189 г исходного ангидрида. Примерно 46 г взятого ангидрида, а также ангидрид ацетоксималеиновой кислоты остаются в виде черной массы в колбе; 15 г исходного ангидрида перегоняются неразложившимися в приемник.
Суммарный выход сырого продукта составляет 32 г. Затем многократной фракционной перегонкой получают 31,5 г недокиси углерода.
Способы получения:
- Реакцией дихлорангидрида диброммалоновой кислоты с цинком в эфирном растворе. (выход 70%) [Лит.]
- Пиролиз ангидрида диацетилвинной кислоты над платиной при 350 С. (выход 40%) [Лит.]
- Пиролиз диэтилоксалилацетата. (выход 48%) [Лит.]
- Реакция малоновой кислоты с пентаоксидом фосфора. (выход 20%) [Лит.]
- Реакция дихлорангидрида малоновой кислоты с оксидом свинца(II). (выход 10%) [Лит.]
Реакции вещества:
- При осторожном окислении недоокиси углерода 2% раствором перманганата калия удалось выделить небольшое количество мезоксалевой кислоты. [Лит.]
- С реактивами Гриньяра в зависимости от соотношения реагентов образуются или бета-дикетоны или метилкетоны. [Лит.]
- С галогеноводородами дает дигалогенангидриды малоновой кислоты. [Лит.]
- Реакцией с хлоридом брома(I) получен дихлорангидрид диброммалоновой кислоты. [Лит.]
- С малоновой кислотой образуется твердый продукт неизвестного строения. [Лит.]
- Реагирует с меркаптанами с образованием эфиров дитиомалоновой кислоты. [Лит.]
- Легко реагирует с муравьиной и уксусной кислотами давая смешанные ангидриды. [Лит.]
- Реакция с безводной щавелевой кислотой дает углекислый, угарный газ и лактон бета-оксиизопропилмалоновой кислоты. [Лит.]
- Со спиртами образует эфиры малоновой кислоты; метиловый и этиловый спирты реагируют при комнатной температуре, начиная с пропилового требуется нагревание и применение катализаторов. [Лит.]
- С первичными аминами легко дает амиды малоновой кислоты. [Лит.]
- С фенилгидразином образуется 1-фенил-3,5-диоксопиразолидин. [Лит.]
- При нагревании с бензамидами получены бис-малонильные производные. [Лит.]
- С ароматическими альдегидами образует арилиденовые эфиры замещенных малоновых кислот. [Лит.]
- Мочевина и тиомочевина реагируют с недоокисью углерода с образованием барбитуровой кислоты и тиобарбитуровой кислоты соответственно. [Лит.]
- В присутствии эквимолекулярных количеств безводного хлорида алюминия недоокись углерода вступает в реакцию Фриделя-Крафтса с бензолом, нафталином и их гомологами с образованием ацетофенонов после гидратации продукта реакции. [Лит.]
- Горит синим, коптящим пламенем. [Лит.]
- Недоокись углерода полимеризуется в присутствии катализаторов. [Лит.1]
- При реакции эфирного раствора метиллития с недоокисью углерода образуется ацетилацетон. Выход 47%. [Лит.1
 ]
]
2CH3Li + C3O2 → CH3C(OLi)=C=C(OLi)CH3
CH3C(OLi)=C=C(OLi)CH3 + 2H2O → CH3COCH2COCH3 + 2LiOH
- При комнатной температуре реакция недоокиси углерода с водой с образованием малоновой кислоты идет довольно медленно. Для ускорения ее проводят при 60-70 С в присутствии каталитических количеств соляной кислоты. Выход 100%. [Лит.1]
C3O2 + 2H2O → CH2(COOH)2
Показатель преломления (для D-линии натрия):
1,4538 (6°C)
Давление паров (в мм рт.ст.):
1 (-94,8°C)
10 (-71°C)
100 (-36,9°C)
573,5 (0°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль):
-93,6 (г)Стандартная энтропия вещества S (298 К, Дж/(моль·K)):
276,1 (г)Стандартная мольная теплоемкость Cp (298 К, Дж/(моль·K)):
66,99 (г)Биологическое действие:
Токсична. Уже в небольших концентрациях действует как лакриматор, в больших вызывает удушье.
Анализ вещества:
ИК-спектр (см-1): 3750 (ср.), 3087 (ср.), 2400 (с.), 2258 (оч. с.), 1669 (ср.), 1575 (ср.), 634 (сл.), 549 (с.).
Дополнительная информация::
В жидком виде легко воспламеняется. Полимеризуется при сжижении или хранении при давлении выше 100 мм.рт.ст. в красный полимер. Полимеризация ускоряется пентаоксидом фосфора, пиридином, триэтиламином.
При взаимодействии с водой в течение 1 часа количественно дает малоновую кислоту.
Источники информации:
- Binneweis M., Milke E. Thermochemical Data of Elements and Compounds. - 2ed, 2002. - С. 267
- Dictionary of organic compounds. - Vol.1, Abadole-Cytosine. - New York, 1953. - С. 428
- Dictionary of organic compounds. - vol.1, Abietic acid - Dypnone. - London, 1946. - С. 398
- The Merck Index. - 11th ed. - Merck & Company, 1989. - С. 275-276
- Некрасов Б.В. Основы общей химии. - Т.1. - М.: Химия, 1973. - С. 513
- Реми Г. Курс неорганической химии. - Т.1. - М., 1963. - С. 481
- Руководство по неорганическому синтезу. - Т.3, под ред. Брауэра Г. - М.: Мир, 1985. - С. 682-684
- Справочник химика. - 2 изд., Т. 2. - Л.-М.: Химия, 1964. - С. 228-229
- Справочник химика. - 2 изд., Т.1. - Л.-М.: Химия, 1966. - С. 605 (давление паров)
- Успехи химии. - 1967. - Т.36, №6. - С. 947-964
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер